Qu'est-ce que la médecine de précision ?
Mis à jour le
La médecine de précision, également appelée médecine personnalisée, a pour objectif de proposer au patient un traitement adapté aux anomalies de sa tumeur. Elle repose actuellement sur deux types de traitements : les thérapies ciblées et l’immunothérapie spécifique.
On sait aujourd’hui qu’il n’existe pas un cancer par organe mais une multitude de sous-types de cancers présentant chacun des anomalies particulières au sein des cellules cancéreuses et de leur environnement. Les traitements de médecine de précision visent à bloquer ou corriger ces perturbations en ciblant les anomalies moléculaires qui en sont responsables.
Les thérapies ciblées ont pour objectif de bloquer la croissance ou la propagation de la tumeur, en interférant avec des anomalies moléculaires ou avec des mécanismes qui sont à l’origine du développement ou de la dissémination des cellules cancéreuses.
Les traitements d’immunothérapie spécifique vont, quant à eux, restaurer l’efficacité du système immunitaire, en agissant sur des cibles particulières de la tumeur ou de son environnement, pour lui permettre de détruire les cellules cancéreuses.
Quelle place par rapport aux autres traitements ?
La médecine de précision fait aujourd’hui partie des soins disponibles contre les cancers. Elle ne remplace pas les traitements déjà en place, tels que la chirurgie, la chimiothérapie ou la radiothérapie mais elle vient compléter l’arsenal thérapeutique existant. La médecine de précision offre ainsi de nouvelles possibilités pour les patients présentant des cancers contre lesquels les traitements « classiques » ne sont pas suffisants (ex : formes avancées de cancers ou rechute à la suite d’un précédent traitement).
Aujourd’hui, la médecine de précision permet de :
- développer de nouveaux traitements ciblant précisément des mécanismes biologiques jouant un rôle majeur dans le développement des tumeurs
- identifier des groupes de patients dont les tumeurs présentent des anomalies moléculaires communes susceptibles d’être ciblées par des traitements spécifiques
Les traitements de la médecine de précision peuvent être utilisés seuls ou en association avec d’autres traitements ciblés, de la chimiothérapie conventionnelle ou encore de la radiothérapie.
Les traitements en pratique
Les thérapies ciblées dites « petites molécules » (type crizotinib, imatinib, afatinib…) sont prises par voie orale sous forme de comprimés ou de gélules (un ou plusieurs comprimés par prise, une ou plusieurs fois par jour).
La prise des traitements par voie orale présente des avantages pour le patient mais requiert une attention particulière. Cette méthode d’administration est effectivement plus simple, le patient pouvant prendre son traitement à domicile, sans nécessité d’hospitalisation. Si les médicaments oraux apportent ainsi un certain confort aux patients, ils ne doivent pas pour autant être considérés comme moins toxiques que les traitements intraveineux administrés à l’hôpital. La gestion des effets indésirables peut s’avérer difficile pour le patient qui se retrouve seul à la maison et pour les professionnels de premier recours qui l’entourent (médecins généralistes, pharmaciens d’officine et infirmiers libéraux). Aussi, le risque de mauvaise observance est réel. Si ces médicaments ne sont pas pris correctement, conformément au protocole de traitement, leur efficacité peut en effet être compromise.
Les anticorps monoclonaux (type bevacizumab, trastuzumab, ipilimumab…), classés parmi les thérapies ciblées ou l’immunothérapie, sont administrés à l’hôpital par perfusion (voie intraveineuse principalement).
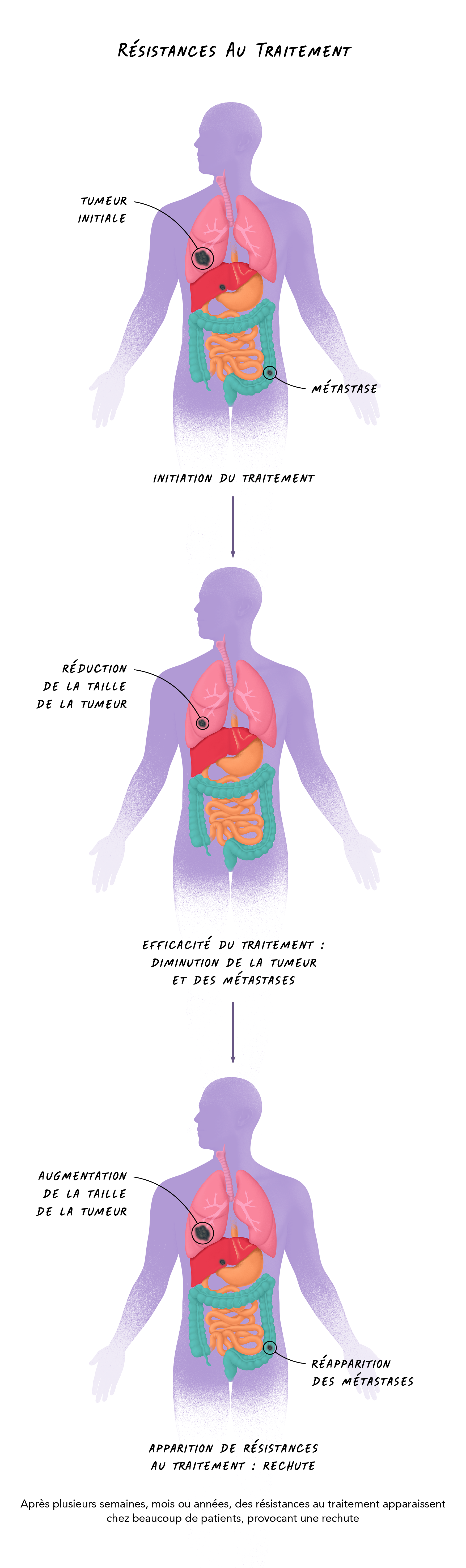
La résistance aux traitements
Chez certains patients, la thérapie prescrite se révèlera inefficace d’emblée. On parlera alors de résistance « primaire » au traitement. D’autres patients vont, en revanche, en tirer un bénéfice thérapeutique immédiat. Il n’est pas rare cependant que la maladie réapparaisse ou se remette à progresser après quelques semaines, mois ou années de traitement. Cela signifie que le médicament n’est plus efficace pour contrer la maladie. On parlera alors de résistance « secondaire » au traitement.
Des résistances peuvent, en effet, survenir lorsque la cible visée par le médicament est modifiée à la suite d’une nouvelle mutation, dans l’ADN des cellules tumorales, qui va limiter l’efficacité du traitement initial. Une autre voie de signalisation, permettant aux cellules tumorales de proliférer indépendamment de la cible du médicament, peut également devenir prépondérante, rendant alors le traitement inefficace.
Par ailleurs, une tumeur n’est pas un amas uniforme de cellules cancéreuses identiques mais se compose en réalité de plusieurs types de cellules en constante évolution. Des études récentes ont montré l’existence, au sein d’une même tumeur, de cellules tumorales présentant des anomalies moléculaires différentes. On parle d’hétérogénéité intratumorale. Pour un même patient, une métastase peut également présenter des anomalies différentes de la tumeur primaire ou d’une autre métastase.
Cette hétérogénéité tumorale a de lourdes conséquences en termes d’efficacité de traitement. Pour être efficace, un traitement devrait en effet pouvoir cibler toutes les cellules tumorales. C’est pour cette raison que beaucoup de médicaments sont prescrits en association, pour pouvoir attaquer la tumeur sur tous les fronts.
Ainsi, comprendre l’hétérogénéité de la tumeur, être capable de contrer les résistances et trouver des stratégies thérapeutiques adaptées sont des voies de recherche majeures pour les prochaines années.