Inhibiteurs de PARP : parcours des patients en génétique oncologique
Mis à jour le
L’olaparib est le premier inhibiteur de PARP à avoir obtenu une AMM européenne. Il est destiné aux patientes atteintes d’un cancer de l’ovaire et porteuses d’une altération BRCA, ainsi qu’aux patients atteints d’un cancer du sein HER2 négatif et porteurs d’une altération BRCA. Les principaux parcours de ces patients en génétique oncologique, conditionnant la prescription d’olaparib, ont été détaillés dans un rapport de l’Institut mis à jour en novembre 2019.
Inhibiteurs PARP : préconisations pour un parcours en génétique oncologique (octobre 2019)
PDF 2 MB
La fréquence élevée des altérations du gène BRCA dans les cancers de l’ovaire et certains cancers du sein, ainsi que le caractère constitutionnel de la majorité d’entre elles, confèrent une portée familiale majeure aux tests génétiques BRCA à mettre en œuvre.
Ainsi, une consultation d’oncogénétique est préconisée dès le diagnostic initial pour toute nouvelle patiente atteinte d’un cancer de l’ovaire, afin qu’elle soit informée des répercussions personnelles et familiales potentielles des résultats des tests BRCA. Cette préconisation s’applique aussi aux patientes atteintes d’un cancer de l’ovaire en situation de rechute et pour lesquelles la consultation d’oncogénétique n’avait pas été réalisée, et depuis 2019, aux patients atteints d’un cancer du sein localement avancé ou métastatique HER2 négatif et présentant des mutations germinales BRCA.
Le type d’altération recherché a un impact fort sur l’organisation qui doit être mise en place. L’objectif de ces préconisations est de définir, selon le type d’altération recherché, l’organisation permettant d’effectuer les tests nécessaires dans un délai compatible avec le traitement des patients et de s’assurer qu’ils disposent de toute l’information nécessaire quant aux répercussions personnelles et familiales potentielles du résultat de ces tests.
Actualisation des recommandations sur les parcours en génétique oncologique
Premier inhibiteur de PARP à avoir obtenu une autorisation de mise sur le marché (AMM) européenne, en 2014, l’olaparib peut être prescrit en traitement d’entretien des patientes atteintes d’un cancer de l’ovaire récidivant, porteuses d’une altération (germinale et/ou somatique) du gène BRCA et en réponse complète ou partielle à une chimiothérapie à base de platine.
À la suite de nouvelles indications attribuées aux inhibiteurs de PARP, l’Institut national du cancer a actualisé fin 2019 ses recommandations concernant les parcours en génétique oncologique.
- Ces préconisations concernent :
le traitement d’entretien en monothérapie des patientes adultes atteintes d’un cancer avancé
épithélial de l’ovaire, des trompes de Fallope ou péritonéal primitif (stades FIGO III et IV) nouvellement diagnostiqué avec altération des gènes BRCA1/2 germinale et/ou somatique et qui sont en réponse partielle ou complète à une première ligne de chimiothérapie à base de platine ; - le traitement d’entretien en monothérapie des patientes adultes atteintes d’un cancer épithélial séreux de haut grade de l’ovaire, des trompes de Fallope ou péritonéal primitif, récidivant et sensible au platine, avec une altération des gènes BRCA1/2 (germinale et/ou somatique) et qui sont en réponse partielle ou complète à une chimiothérapie à base de platine ;
- le traitement en monothérapie des patients adultes atteints d’un cancer du sein localement avancé ou métastatique HER2 négatif et présentant des mutations germinales BRCA1/2, ayant déjà reçu un traitement (néo)adjuvant par une anthracycline et/ou un taxane, sauf s’ils n’étaient pas éligibles à ce type de traitement. Les patients atteints d’un cancer du sein positif aux récepteurs hormonaux (RH) doivent préalablement avoir reçu une hormonothérapie ou être considérés comme non-éligibles à une hormonothérapie.
Actuellement, et selon les indications, les prescriptions d’olaparib :
- sont conditionnées par la présence d’une altération BRCA tumorale et/ou constitutionnelle ;
- conditionnées par la présence d’une altération BRCA constitutionnelle ;
- ne sont pas conditionnées par la présence d’une altération.
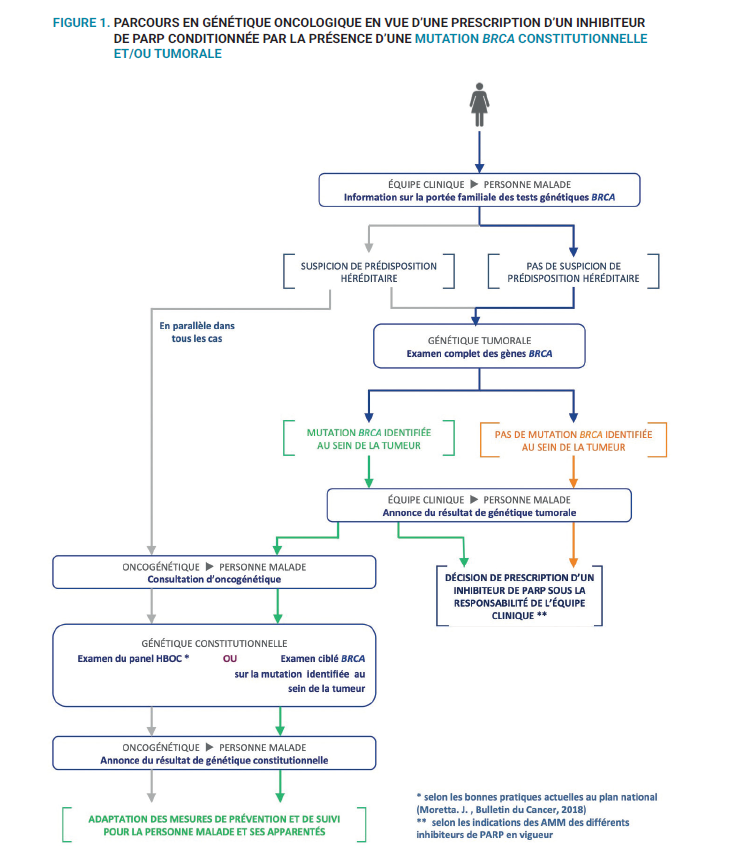
Prescription d'un inhibiteur de PARP conditionnée par la présence d'une mutation BRCA tumorale et/ou constitutionnelle
Sont actuellement concernés :
- le traitement d’entretien en monothérapie des patientes adultes atteintes d’un cancer avancé épithélial de l'ovaire, des trompes de Fallope ou péritonéal primitif (stades FIGO III et IV) nouvellement diagnostiqué avec altération des gènes BRCA1/2 germinale et/ou somatique et qui sont en réponse partielle ou complète à une première ligne de chimiothérapie à base de platine ;
- le traitement d'entretien en monothérapie des patientes adultes atteintes d’un cancer épithélial séreux de haut grade de l'ovaire, des trompes de Fallope ou péritonéal primitif, récidivant et sensible au platine avec une altération des gènes BRCA1/2 germinale et/ou somatique et qui sont en réponse partielle ou complète à une chimiothérapie à base de platine.
Le parcours sera orienté selon l’existence ou non de critères individuels et/ou familiaux susceptibles d’évoquer une prédisposition héréditaire aux cancers. En conséquence, l’équipe clinique doit être associée à une équipe d’oncogénétique et un partenariat est à formaliser pour permettre notamment de retenir les critères familiaux évocateurs d’une prédisposition génétique au cancer.
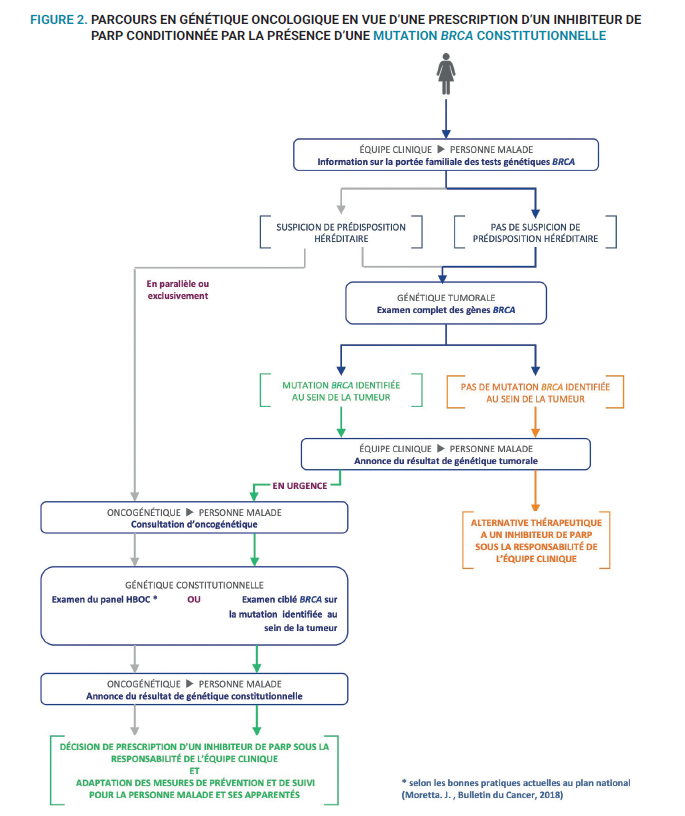
Prescription d'un inhibiteur de PARP conditionnée par la présence d'une mutation BRCA constitutionnelle
- Est actuellement concerné :
le traitement en monothérapie des patients adultes atteints d’un cancer du sein localement avancé ou métastatique HER2 négatif et présentant des mutations germinales BRCA1/2 :- les patients doivent avoir déjà reçu un traitement (néo)adjuvant par une anthracycline et/ou un taxane pour un cancer localement avancé ou métastatique, sauf s’ils n’étaient pas éligibles à ce type de traitement ;
- les patients atteints d’un cancer du sein positif aux récepteurs hormonaux (RH) doivent préalablement avoir reçu une hormonothérapie ou être considérés comme non-éligibles à une hormonothérapie.
Le parcours sera orienté selon l’existence ou non de critères individuels et/ou familiaux
susceptibles d’évoquer une prédisposition héréditaire aux cancers. En conséquence,
l’équipe clinique doit être associée à une équipe d’oncogénétique et un partenariat est
à formaliser permettant, notamment, de retenir les critères familiaux évocateurs d’une
prédisposition génétique au cancer.